O przebiegu procesu dysocjacji decyduje rozpuszczalnik. Substancje, które w środowisku wodnym są elektrolitami mocnymi, w innych rozpuszczalnikach mogą być słabymi i odwrotnie.
Woda jako bardzo słaby elektrolit ulega w niewielkim stopniu procesowi dysocjacji elektrolitycznej (autodysocjacja).
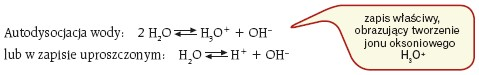
Stosując do tej równowagi prawo działania mas, można wprowadzić pojęcie iloczynu jonowego wody jako iloczynu stężeń jonów wodorowych i wodorotlenkowych:
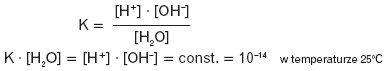
Iloczyn ten jest wielkością stałą w danej temperaturze:
![]()
Definiując kolejne pojęcia (wielkości charakteryzujące odczyn roztworu) pH i pOH:
![]()
otrzymujemy zależność:
![]()
Odczyn roztworu zależy od stężenia jonów H+ i stężenia jonów OH–.
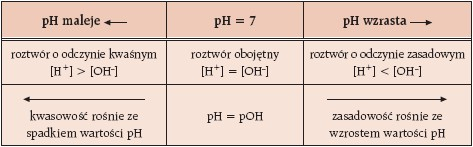
Wskaźniki kwasowo-zasadowe to związki typu słabych kwasów lub słabych zasad organicznych. Barwa ich formy zdysocjowanej i niezdysocjowanej jest różna. pH roztworu decyduje, która z tych form będzie w przewadze i która barwa wskaźnika się pojawi. W roztworze ustala się stan równowagi, którego położenie zależy od stężenia jonów H+ i OH–. W przypadku wskaźnika będącego słabym kwasem, np. oranżu metylowego, forma zdysocjowana nadaje roztworowi barwę żółtą, a niezdysocjowana – czerwoną:
![]()
W środowisku zasadowym jony OH– spowodują przesunięcie równowagi w prawo, co wywoła zmianę barwy wskaźnika.
Przykłady wskaźników kwasowo-zasadowych:
| wskaźnik | barwa w środowisku | zakres pH zmiany barwy | |
| kwasowym | zasadowym | ||
| błękit tymolowy | czerwona | żółta | 1,2 – 2,8 |
| błękit bromokrezolowy | żółta | niebieska | 3,0 – 4,6 |
| czerwień Kongo | niebieska | czerwona | 3,0 – 5,0 |
| oranż metylowy | czerwona | żółta | 3,2 – 4,4 |
| zieleń bromokrezolowa | żółta | niebieska | 3,8 – 5,2 |
| błękit bromotymolowy | żółta | niebieska | 6,0 – 7,6 |
| lakmus | czerwona | niebieska | 4,5 – 8,3 |
| fenoloftaleina | bezbarwna | malinowa | 8,2 – 10,0 |
Najpopularniejszym wskaźnikiem jest papierek uniwersalny nasycony mieszaniną wskaźników, zwany wskaźnikowym, który w roztworze o odczynie kwasowym przyjmuje barwę czerwoną, o odczynie zasadowym – niebiesko - zieloną, a w roztworze o odczynie obojętnym jego barwa pozostaje bez zmian, czyli żółta.
Jak zbadać odczyn roztworu? Należy nanieść kroplę roztworu na uniwersalny papierek wskaźnikowy:
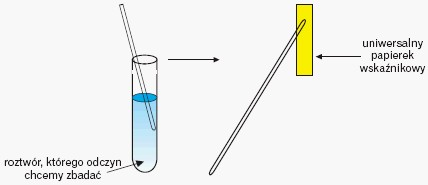
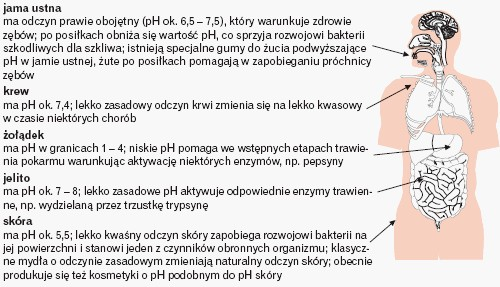
Warto zwrócić uwagę, że odpowiednie pH warunkuje też prawidłowe działanie organizmu ludzkiego. W każdym narządzie pH ma odpowiednią wartość, która powoduje, że działające w nim enzymy są aktywne. Wartość pH płynów ustrojowych lub jam ciała odgrywa także rolę w obronie organizmu przed bakteriami i wirusami.