Widmo jest rozkładem promieniowania elektromagnetycznego na zbiór elementarnych fal o różnej długości. Na podstawie analizy widma można badać różne substancje w celu identyfikacji pierwiastków, które się w nich znajdują. Jest to możliwe dzięki temu,że atom każdego pierwiastka ze względu na swoją budowę może emitować lub absorbować fale elektromagnetyczne charakterystyczne tylko dla niego.
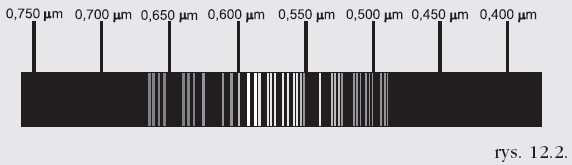
Widmo emisyjne atomu danego pierwiastka to zbiór fal elektromagnetycznych o określonych długościach wysyłanych prze zatom tego pierwiastka podczas przejść elektronu z wyższych poziomów energetycznych na niższe. Przykład takiego widma przedstawiony jest na rys.12.2. Jest to widmo liniowe wysyłane przez zmuszone do świecenia atomy baru.
Widmo absorpcyjne danego pierwiastka powstaje wtedy, gdy na drodze promieniowania elektromagnetycznego o widmie ciągłym znajdzie się substancja (np. wodór w stanie gazowym) pochłaniająca promieniowanie powodując, że widmo pochodzące od źródła pozbawione zostaje tych długości fal, które pochłonięte zostały przez ciało.
Widma dzielimy na następujące rodzaje:
- widma liniowe wysyłane przez pojedyncze atomy określonego pierwiastka – takie widmo uzyskujemy badając dany pierwiastek w stanie gazowym, pod niskim ciśnieniem,
- widma pasmowe wysyłane przez całe cząsteczki związków chemicznych,
- widma ciągłe wysyłane przez ciała stałe i ciekłe oraz gazy pod dużym ciśnieniem.
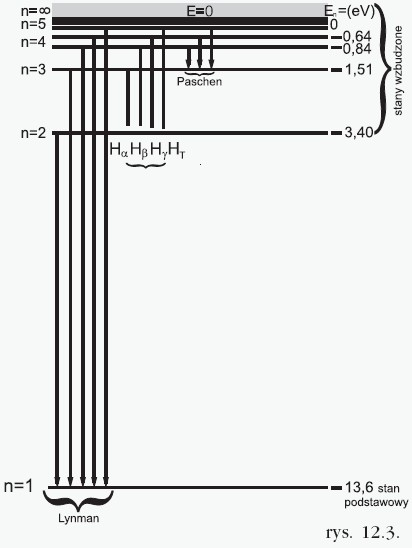
Widmo atomu wodoru tak samo jak widmo określające pojedyncze atomy każdego innego pierwiastka jest widmem liniowym. Długość fali każdej z linii widma atomu wodoru da się obliczyć z następującego wzoru:
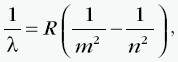
gdzie R – jest stałą Rydberga równą 1097,37 1/m, m to powłoka, na którą przeskoczył elektron, n to powłoka, z której przeskoczył elektron, λ – długość fali.
W widmie wodoru wyróżnić można 3 podstawowe serie, które związane są z przejściami elektronu pomiędzy określonymi orbitami:
- Seria Laymana związana jest z przeskokami elektronu na powłokę podstawową z wyższych powłok. Seria ta należy do zakresu widma rentgenowskiego (dla tej serii m = 1, a n = 2, 3, 4, ...).
- Seria Balmera związana jest z przeskokami elektronu na drugą powłokę z powłok wyższych. Seria ta należy do zakresu widma widzialnego(dla tej serii m = 2,a n = 3, 4, 5, ...).
- Seria Parshena związana jest z przeskokami elektronu na trzecią powłokę z powłok wyższych (dla tej serii m = 3, a n = 4, 5, 6, ...).