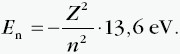Teoria budowy atomu sformułowana przez Bohra z punktu widzenia współczesnej fizyki jest błędna. Jednak postulaty tej teorii prowadzą do wniosków, które dobrze służą do opisu atomów wodoropodobnych.
Przed stworzeniem przez Bohra teorii atomu Ernest Rutherford na podstawie swoich doświadczeń wyprowadził wniosek, że atom składa się z dodatnio naładowanego jądra atomowego oraz ujemnie naładowanych elektronów, które poruszają się wokół jądra po orbitach kołowych i eliptycznych. Zgodnie z mechaniką klasyczną oraz elektrodynamiką elektrony poddawane przyspieszeniom podczas takiego ruchu wokół jądra powinny emitować fale elektromagnetyczne i tracić energię. Utrata energii związana ze zmniejszeniem prędkości powodowałaby, że elektrony zmniejszałyby także promień obiegu wokół jądra. Ostatecznie doprowadziłoby to do niewystępującego w rzeczywistości szybkiego upadku elektronu na jądro. Postulaty wprowadzone przez Bohra powodują, że w jego teorii nie występują sprzeczne z doświadczeniem wnioski.
Elektron, który znajduje się najbliżej jądra, czyli na najniższej dozwolonej orbicie, ma najmniejszą energię i jest w stanie podstawowym. Kiedy energia elektronu jest większa, to jest on w stanie wzbudzonym.
Elektrony dążą do zajęcia stanów o najniższej energii i gdy znajdą się w stanie wzbudzonym, to przechodzą do stanu podstawowego wysyłając nadmiar energii.
Jednostką energii stosowaną w fizyce atomowej jest 1 elektronovolt [eV], który jest równy energii kinetycznej, jaką uzyska elektron przechodząc między punktami pola elektrycznego o różnicy potencjałów równej 1 V. (1 eV = 1,6 · 10-19 J)
Można zauważyć, że we wzorze na energię elektronu znajdującego się na n-tej powłoce da się wydzielić wyrażenie które jest wielkością stałą. Po wyznaczeniu wartości tego wyrażenia otrzymujemy następujący wzór na energię związaną z n-tą powłoką: