- działanie kwasem siarkowym(VI) na metanian sodu w celu otrzymania kwasu metanowego
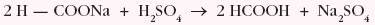
- katalityczne utlenianie etanalu do kwasu etanowego

- fermentacja octowa, którą sumarycznie można zapisać
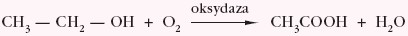
- utlenianie metylobenzenu i etylobenzenu manganianem(VII) potasu w odpowiednim środowisku prowadzi do otrzymania kwasu benzoesowego, co przedstawiono schematycznie poniżej:
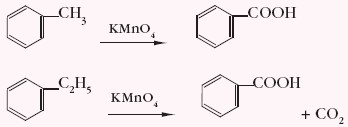
Analizując budowę cząsteczki kwasu metanowego można wyciągnąć wniosek, że kwas ten posiada właściwości redukujące i daje pozytywny wynik próby Tollensa i Trommera.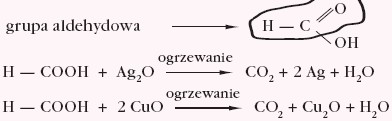
Kwas metanowy pod wpływem stężonego kwasu siarkowego(VI) ulega odwodnieniu tworząc tlenek węgla(II) i wodę.
O właściwościach kwasów decyduje również charakter reszty węglowodorowej. Jeżeli grupa ta ma charakter nienasycony, to uzyskamy pozytywny wynik reakcji z manganianem(VII) potasu i wodą bromową. Poniżej przedstawiono schematycznie przebieg tych reakcji z udziałem kwasu 9-oktadecenowego: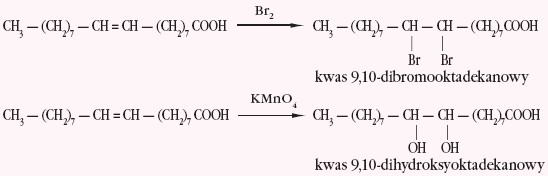
Ten nienasycony kwas w obecności katalizatora przyłączy wodór tworząc kwas nasycony: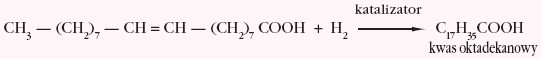
Jeżeli grupa węglowodorowa zawiera pierścień benzenowy, to kwas ten posiada charakter aromatyczny i ulega np. nitrowaniu. Ponieważ grupa karboksylowa należy do podstawników II rodzaju, powstaje izomer meta, np.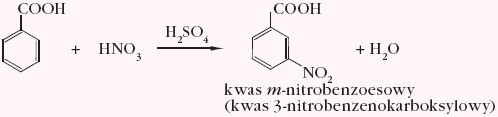
Kwas benzoesowy jest kwasem mocniejszym od etanowego, ale słabszym od metanowego.
Kwas etanodiowy, zwany szczawiowym, należy do kwasów dikarboksylowych:![]()
Ze względu na obecność dwóch grup karboksylowych jego moc zwiększa się w stosunku do kwasu metanowego. Kwas ten można otrzymać podczas utleniania etynu manganianem(VII) potasu w określonych warunkach, co można przedstawić ogólnym schematem:![]()
Reakcją pozwalającą na wykrycie jonów etanodiowych (szczawianowych) C2O42– w roztworze jest reakcja z jonami wapnia Ca2+, w wynikuktórej strąca się biały osad etanodianu (szczawianu) wapnia:![]()

