Alkohole to związki zawierające grupę funkcyjną –OH związaną z tetraedrycznym atomem węgla. Grupa –OH nosi nazwę grupy hydroksylowej.
R-OH to ogólny wzór alifatycznych alkoholi monohydroksylowych. Istnieją różnorodne sposoby klasyfikacji alkoholi, np.
- w zależności od tego, czy grupa –OH związana jest z pierwszorzędowym, drugorzędowym, czy trzeciorzędowym atomem węgla wyróżniamy alkohole I-rzędowe, II-rzędowe i odpowiednio III-rzędowe, np.
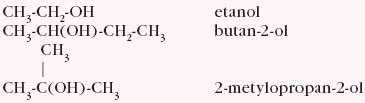
Rzędowość alkoholi wpływa znacząco na ich właściwości chemiczne. - w zależności od liczby grup –OH w cząsteczce związku wyróżniamy alkohole monohydroksylowe lub polihydroksylowe, np.
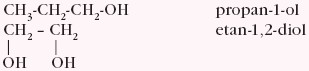
- w zależności od charakteru reszty węglowodorowej:
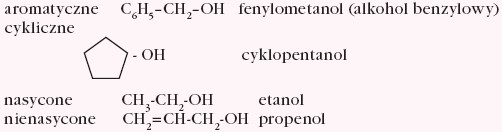
Obecność grup –OH i możliwość tworzenia wiązań wodorowych pomiędzy cząsteczkami alkoholi prowadzi do asocjacji cząsteczek. Stąd nasycone alkohole monohydroksylowe mają temperatury wrzenia i topnienia odpowiednio wyższe od temperatur wrzenia i topnienia węglowodorów o tej samej liczbie atomów węgla w cząsteczce.
Ze wzrostem liczby atomów węgla w łańcuchu, czyli ze wzrostem wpływu tego łańcucha na właściwości związku (długi łańcuch węglowodorowy jest dominującą częścią cząsteczki) maleje rozpuszczalność w wodzie, jak i reaktywność alkoholi. Wyższe alkohole dobrze rozpuszczają się w heksanie i innych węglowodorach. Alkohole mają odczyn obojętny, a w roztworze wodnym nie ulegają dysocjacji elektrolitycznej.
Alkohole reagują:
- z metalami aktywnymi (sód, potas, magnez, na gorąco – wapń), tworząc alkoholany, np.
CH3CH2OH + Na → CH3CH2ONa + 1/2 H2
- łatwość rozerwania wiązania RO-H maleje w kierunku: alkohol I-rzędowy > alkohol II-rzędowy > alkohol III-rzędowy
- powstające alkoholany ulegają hydrolizie anionowej (jak sól mocnej zasady i słabego kwasu), np. wodny roztwór etanolanu sodu ma odczyn zasadowy, co potwierdza jonowy zapis tego procesu:
CH3CH2O– + H2O → CH3CH2OH + OH–
- z halogenowodorami (HX = HCl, HBr, HI), tworząc halogenki alkilowe:
CH3CH2OH + HX → CH3CH2X + H2O
- podstawianie grupy –OH zachodzi najłatwiej dla alkoholi III-rzędowych
- z kwasami organicznymi lub nieorganicznymi, tworząc estry
Alkohole ulegają:
- odwodnieniu (eliminacji wody) tworząc – w wysokiej temperaturze i w obecności katalizatora (Al2O3) – alkeny, np.
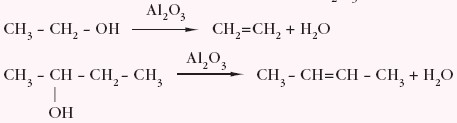
- eliminacja wody zachodzi zgodnie z regułą Zajcewa
- reakcji odwodnienia 2 cząsteczek w obecności kwasu H2SO4,w której powstają etery
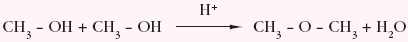
- łagodnemu utlenianiu podczas ogrzewania, np.
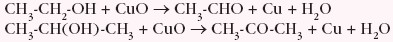
- alkohole I-rzędowe utleniają się do aldehydów
- alkohole II-rzędowe utleniają się do ketonów
- utlenianie alkoholi III-rzędowych zachodzi trudno i prowadzi do rozpadu cząsteczek na mniejsze fragmenty

