Poniżej zamieszczono tabelę zawierającą informacje na temat właściwości fizycznych wybranych nasyconych kwasów jednokarboksylowych:
| nazwa | TT[0C] | TW [0C] | właściwości fizyczne |
| kwas metanowy (mrówkowy) |
8,30 | 100,7 | bezbarwna ciecz o charakterystycznym zapachu, miesza się z wodą, etanolem i eterem w każdym stosunku |
| kwas etanowy (octowy) |
16,63 | 117,9 | bezbarwna, żrąca ciecz o charakterystycznym zapachu octu, dobrze rozpuszczalna w wodzie, etanolu, eterze |
| kwas butanowy (masłowy) |
–4,30 | 163,3 | bezbarwna oleista ciecz o gorzkim smaku i zapachu zepsutego masła, rozpuszczalna w wodzie, eterze i etanolu |
| kwas pentanowy (walerianowy) |
–33,8 | 186,3 | ciecz o nieprzyjemnym zapachu |
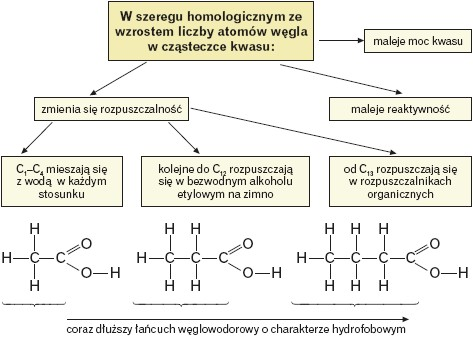
Ze wzrostem długości łańcucha węglowego o charakterze hydrofobowym maleje rozpuszczalność kwasu w wodzie; cząsteczka staje się coraz bardziej hydrofobowa (apolarna) (wiązania węgiel-wodór należą do wiązań atomowych niespolaryzowanych).
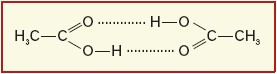
Polarność wiązań w grupie karboksylowej powoduje, że pomiędzy cząsteczkami kwasów karboksylowych występują wiązania wodorowe. Obecność wiązań wodorowych wywołuje stosunkowo wysokie temperatury wrzenia tych związków, jak również wpływa na rozpuszczalność w wodzie. Asocjacja cząsteczek występuje nie tylko w fazie ciekłej, alei gazowej. Kwas etanowy w fazie gazowej występuje w postaci cyklicznego dimeru.