Mangan jest pierwiastkiem aktywnym chemicznie. W postaci rozdrobnionej spala się w tlenie, tworząc mieszaninę tlenków MnO2 i Mn3O4, reaguje z gorącą wodą oraz kwasami słabo utleniającymi.
![]()
Roztwory wodne rozpuszczalnych soli manganu(II) są praktycznie bezbarwne. Siarczek manganu(II) to cielisty osad.
![]()
Mangan tworzy trzy podstawowe tlenki: tlenek manganu(II) MnO, tlenek manganu(IV)MnO2 i tlenek manganu(VII) Mn2O7, które można otrzymać w następujących reakcjach:
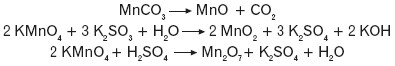
Charakter chemiczny tych tlenków zmienia się wraz ze zmianą stopnia utlenienia manganu.

Mangan tworzy wodorotlenek Mn(OH)2.
Świeżo strącony biały osad wodorotlenku manganu(II) pod wpływem tlenu z powietrza lub nadtlenku wodoru brunatnieje wskutek utleniania.
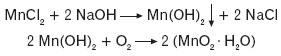
Wodorotlenek manganu(II) posiada charakter zasadowy, czyli reaguje z kwasami.
![]()
Tlenek manganu(IV) – brunatny osad – jest silnym utleniaczem. W reakcjach z kwasami następuje redukcja MnIV do MnII.
![]()
Podczas ogrzewania MnO2 rozkłada się z wydzieleniem tlenu:
![]()
Podczas stapiania tlenku manganu(IV) z wodorotlenkami litowców przy dostępie powietrza powstają sole manganiany(VI).
![]()
Reakcja opisana powyższym równaniem potwierdza charakter amfoteryczny MnO2. Manganiany(VI) powstają również podczas stapiania tlenku manganu(IV) z azotanem(V) potasu i węglanem potasu:
![]()
W roztworach wodnych manganiany(VI) mają barwę zieloną. W środowisku kwaśnym ulegają dysproporcjonowaniu, dlatego trwałe są tylko w środowisku zasadowym:
![]()
Tlenek manganu(VII), reagując z zasadami, tworzy sole nietrwałego kwasu manganowego(VII) – manganiany(VII), np. manganian(VII) potasu KMnO4. Sól ta jest wykorzystywana do laboratoryjnego otrzymywania tlenu:
![]()
Stosuje się ją także do otrzymywania gazowego chloru:
![]()
Manganian(VII) potasu jako jeden z najsilniejszych utleniaczy łatwo się redukuje, a produkt reakcji zależy od pH roztworu.
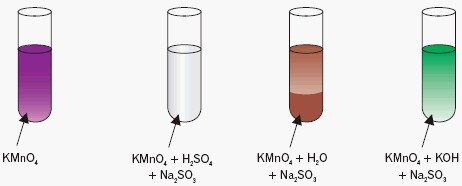
- redukcja w środowisku kwaśnym (odbarwienie fioletowego roztworu):
![]()
- redukcja w środowisku obojętnym (wytrąca się brunatny osad):
![]()
- redukcja w środowisku zasadowym (zmiana barwy roztworu z fioletowej na zieloną):
![]()
Podsumowując powyższe równania reakcji można stwierdzić, że właściwości utleniająco-redukujące związków manganu zmieniają się ze zmianą stopnia utlenienia manganu w związku:
- związki manganu(II) są reduktorami,
- tlenek manganu(IV) w zależności od doboru pozostałych substratów może pełnić zarówno rolę utleniacza, jak i reduktora,
- związki manganu(VII) są utleniaczami.

